*Judul Percobaan : Reaksi
Eksoterm dan Endoterm
*Tujuan Percobaan : Mengetahui Reaksi
Eksoterm dan Endoterm
*Landasan Teori
:
Reaksi
Eksoterm dan Reaksi Endoterm
Perubahan entalpi (ΔH) positif menunjukkan
bahwa dalam perubahan terdapat penyerapan kalor atau pelepasan kalor. Reaksi
kimia yang melepaskan atau mengeluarkan kalor disebut reaksi eksoterm,
sedangkan reaksi kimia yang menyerap kalor disebut reaksi endoterm. Aliran kalor
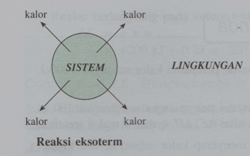
pada kedua jenis reaksi diatas dapat dilihat pada gambar berikut:
A. REAKSI
EKSOTERM
Reaksi eksoterm adalah reaksi yang melepaskan
kalor. Reaksi eksoterm merupakan reaksi yang disertai dengan perpindahan kalor
dari sistem ke lingkungan ( kalor dibebaskan oleh sistem ke lingkungannya )
ditandai dengan adanya kenaikan suhu lingkungan di sekitar sistem.
Contoh
reaksi eksoterm adalah gamping atau kapur tohor, CaO(s) dimasukkan ke dalam
air.
CaO(s)
+ H2O(l) → Ca(OH)2(aq)
Selain itu, contoh reaksi eksoterm dikehidupan
sehari-hari adalah membakar minyak tanah di kompor minyak dan nyala
api unggun.
Pada reaksi eksoterm , sistem membebaskan energi,
sehingga entalpi sistem akan berkurang, artinya entalpi produk lebih kecil
daripada entalpi pereaksi. Oleh karena itu , perubahan entalpinya bertanda
negatif. Sehingga p dapat dinyatakan sebagai berikut:
ΔH = Hp
–Hr < 0 (negatif)
Perubahan
entalpi pada reaksi eksoterm dapat dinyatakan dengan diagram tingkat energi
seperti berikut ini:
B. REAKSI
ENDOTERM
Reaksi
endoterm adalah reaksi
yang menyerap kalor. Reaksi endoterm merupakan reaksi yang disertai dengan
perpindahan kalor dari lingkungan ke sistem ( kalor diserap oleh sistem dari
lingkungannya )dan ditandai dengan adanya penurunan suhu lingkungan di sekitar
sistem.
Contoh
reaksi endoterm adalah pelarutan amonium khlorida, NH4Cl.
NH4Cl(s)
+ Air → NH4Cl(aq)
Selain itu, contoh lain dari reaksi endoterm yakni
proses fotosintesis pada tumbuhan dan asimilasi.
Pada reaksi endoterm, sistem menyerap energi. Oleh
karena itu, entalpi sistem akan bertambah. Artinya entalpi produk (Hp) lebih
besar daripada entalpi pereaksi (Hr). Akibatnya, perubahan entalpi, merupakan
selisih antara entalpi produk dengan entalpi pereaksi (Hp -Hr) bertanda
positif. Sehingga perubahan entalpi untuk reaksi endoterm dapat dinyatakan:
ΔH = Hp- Hr > 0 (Positif)
Perubahan
entalpi pada reaksi endoterm dapat dinyatakan dengan diagram tingkat energi
seperti berikut ini:
Alat
:
1. Tabung Reaksi
2. Rak Tabung Reaksi
3. Alat Pengaduk (Agar Bahan Menjadi
Larut)
4. Termometer
Bahan :
1. NaOH
2. CO(NH2)2 (Urea)
3. BaCl2
4. CaCl2
5. CuSO4
6. Na2S203
7. Air (Air Murni)
Cara Kerja:
1·
Siapkan alat dan bahan
2·
Letakkan tabung-tabung reaksi di rak tabung reaksi
3·
Ukur dan catatlah suhu air yang akan digunakan sebagai pelarut terlebih dahulu
menggunakan thermometer
4·
Isi tiap-tiap tabung reaksi dengan larutan yang berbeda-beda (Larutan NaOH,
larutan CO(NH2)2, larutan BaCl2, larutan CaCl2, larutan CuSO4, dan larutan Na2S203
5·
Kemudian ukur suhu masing-masing larutan menggunakan thermometer
6·
Catat suhu masing-masing larutan
7.
Jika suhu reaksi mengalami peningkatan, maka reaksi tersebut merupakan reaksi
eksoterm
8·
Jika suhu reaksi mengalami penurunan, maka reaksi tersebut merupakan reaksi
endoterm
TABEL
PENGAMATAN
Keterangan : “Suhu air adalah
29˚C
KESIMPULAN :
Berdasarkan
percobaan yang telah dilakukan, maka kami dapat menyimpulkan bahwa reaksi
eksoterm ditandai dengan kenaikan suhu (keadaan tabung menjadi panas, dan
reaksi endoterm ditandai dengan penurunan suhu (keadaan tabung menjadi dingin).
Adapun zat yang mengalami reaksi eksoterm setelah dilarutkan dalam air antara
lain NaOH, BaCL2, CaCl2,dan CuSO4. Sedangkan zat yang mengalami reaksi endoterm
setelah dilarutkan dalam air yaitu CO(NH2)2dan Na2S2O3.
*Semoga artikel ini bermanfaat, terima kasih sudah membaca*
RM




















.jpg)

3 komentar:
apa yang memengaruhi prakrikum ini, retno? apakah suhu? atau yang lainnya,
mkasih sudah membantu
Kak itu larutan NaOH nya gak ada ledakan ?
Posting Komentar